latihan dan kuis
A. LATIHAN
Jawab :
CFC ini berasal dari mesin pendingin, gas aerosol, dan produk plastik.
Ketika CFC terkena sinar ultraviolet di atmosfer, senyawa itu terurai menjadi senyawa yang mengandung klorin.
Saat klorin bereaksi dengan molekul oksigen pada ozon, molekul ozon juga jadi terurai.
2. Jelaskan proses yang mengakibatkan pemanasan stratosfer.
Jawab :
Jawab :
terjadi perubahan iklim walaupun secara waktu tidak terus menerus terjadi. Namun dalam skala waktu tertentu terjadi perubahan. Hal ini seperti ketika gunung Krakatau meletus pada abad ke 18. Gas aerosol dan debu meluncur ke udara dengan volume yang sangat besar akhirnya menutupi atmosfer bumi. Atmosfer yang tertutup berdampak pada tertutupnya sinar matahari yang kemudian berdampak pada perubahan iklim di bawahnya.
4. Lapisan ionosfer memiliki peranan sangat penting, yaitu:
A. Penyerap utama radiasi ultraviolet
B. Memantulkan gelombang radio yang dipancarkan dan menahan sebagian radiasi matahari
C. Melepas molekul bebas keluar bumi
D. Memantulkan gelombang suara dan menyebarkan radiasi matahari
E. Meneruskan gelombang suara dan menahan radiasi matahari
Pastinya, saat belajar mengenai atmosfer, kamu sudah mengetahui peranan masing-masing lapisan atmosfer. Untuk soal di atas, kamu harus benar-benar mengetahui apa itu ionosfer dan lingkup peranannya di dalam lapisan atmosfer bumi.
Lapisan ionosfer itu memiliki tiga lapisan lainnya, yakni lapisan yang memantulkan gelombang panjang, gelombang menengah, dan gelombang pendek. Ketiga lapisan tersebut menjadi lapisan lalu lintasnya gelombang radio. Selain itu, ketiga lapisan itu menjadi lapisan pelindung radiasi matahari atau ultraviolet setelah Ozonsfer.
Oleh sebab itu, peranan ionosfer dalam lapisan atmosfer bumi ialah memantulkan gelombang radio yang dipancarkan dan kedua menahan sebagian radiasi matahari yang masuk ke bumi. Dengan demikian, jawaban yang tepat untuk soal tersebut ialah B.
b. kuis
1. Data
percobaan dari reaksi : NH4+ (aq) + NO (aq) N2 (aq) + 2H2O (l)
Tentukan rumus kecepatan reaksi berdasarkan percobaan diatas!
Penyelesaian :
Gambar 2
Maka :
Rumus kecepatan reaksinya adalah = r = k[NO2-][NH4+]2
2. Dari
reaksi : 2NO (g) + 2H2 (g) N2 (g) + 2H2O (g) Diperoleh data sebagai
berikut :
Gambar3
a. Tentukan Orde reaksi dari data di atas!
b. Tentukan persamaan laju reaksi tersebut!
Penyelesaian :
a. Gambar4
Reaksi terhadap NO orde = 1
Reaksi terhadap H2 orde = 1
Orde reaksi = 1 + 1 = 2
b. Menentukan pangkat reaksi NO, dengan laju reaksi untuk H2 tetap.
Menentukan pangkat reaksi H2, laju reaksi untuk [NO] tetap
Jadi persamaan laju reaksinya adalah : V = k [NO]
[H2]
1.
Tetapan
kesetimbangan dari reaksi SnO2 + 2H2(g) ⇔
Sn(s) + 2H2O(l) adalah ….
a. Kc = [H2O]2/[H2]2
b. Kc =
[Sn][H2O]2/[Sn][H2]2
c. Kc = [Sn]/[SnO2]
d. Kc = [2H2O]/[2H2]
e. Kc = [H2O]2/[SnO2] [H2]2
alasan :
misal aA + bB <-> cC
+ dD
kc= (C)c (D)d
/ (A)a (B)b
1. Derajat keasaman dari larutan 100 ml H2SO4 0,02 M adalah . . . .
a. 2 – log 4
b. 2 + log 4
c. 2 + log 2
d. 12 + log 4
e. 12
Pembahasan:
H2SO4 merupakan asam kuat, bervalensi 2
[H+] = Ma x Val
= 0,02 x 2 = 4 x 10-2
pH = -log 4 X 10-2
= 2-log 4
Jawaban: A
2. Berapakah konsentrasi ion [OH–] dalam larutan jika konsentrasi H+ = 2 X 10-4 M (Diketahui Kw = 10-14)…….
a. 5 X 10-10
b. 5 X 10-18
c. 0,2 X 10-10
d. 0,2 X 10-8
e. 2 X 10-10
Pembahasan:
Dalam larutan dengan pelarut air, berlaku :
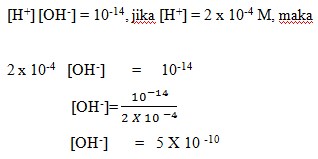
Jawaban: A
8. Larutan asam lemah NH4OH 0,1 M,dan Kb = 10-5 , nilai pH larutan tersebut adalah… . .
a. 11
b. 3
c. 9
d. 14
e. 6
1. Larutan CH3COOH 0,1 M terionisasi dengan derajat ionisasi α= 0,01 mempunyai pH sebesar…..
a. 1
b. 2
c. 3
d. 4
e. 5
Penyelesaian :
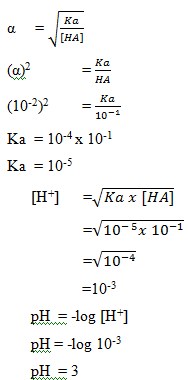
Jawaban : C
2. Terdapat 100 mL larutan NH4OH 0,1 M, Kb NH4OH = 10-5. Maka konsentrasi ion OH– adalah…..
a. 10-3 M
b. 10-1 M
c. 10-2 M
d. 10-6 M
e. 10-5 M
Penyelesaian :
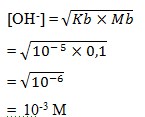
Jawaban : A
2. Sebuah mesin pesawat mengambil 9200 J panas dan membuang 6000 J setiap siklus. a) Berapa kerja mekanik keluaran dari mesin setiap siklus? b) Berapa efisiensi termal dari mesin?
1. Bila diketahui potensial elektrode standar dari :
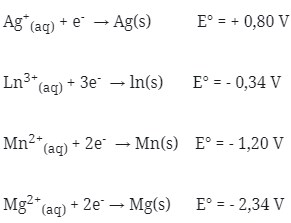
Pasangan sel volta yang akan menghasilkan potensial sel sebesar 0,86 V adalah …
a. ln|ln3+||3Ag+|3Ag
b. Mg|Mg2+||Mn2+|Mn
c. Mn|Mn2+||2Ag+|Ag
d. 2ln|2ln3+||3Mn2+|3Mn
e. 3Mn|3Mn2+||2ln3+|2ln
Jawaban : E
Pembahasan :
Dicari satu persatu potensial sel dari pilihan jawaban
(a) E°sel = E°katode – E°anode
= +0,80 – (- 0,34 ) = 1,14 V
(b) E°sel = E°katode – E°anode
= -1,20 – (-2,34) = 1,14 V
(c) E°sel = E°katode – E°anode
= + 0,80 – (-1,20) = 2 V
(d) E°sel = E°katode – E°anode
= – 1,20 – (- 0,34) = – 0,86 V
(e) E°sel = E°katode – E°anode
= – 0,34 – (- 1,20) = 0,86 V
Jadi, jawaban yang benar adalah E
2. Diketahui :
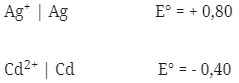
Potensial sel yang dihasilkan dari pasangan elektrode Cd dengan Ag adalah …
a. 0,40 V
b. 0,44 V
c. 0,76 V
d. 0,80 V
e. 1,20 V
Jawaban : E
Pembahasan :
Logam yang memiliki E° lebih kecil selalu merupakan anode (mengalami oksidasi) berarti yang sebagai anode Cd dan sebagai katode Ag.
Notasi Selnya :
Cd|Cd2+||Ag+|Ag
E°sel = E°katode – E°anode
= + 0,80 – (-0,40)
= 1,20 V








Tidak ada komentar:
Posting Komentar